एस ब्लॉक तत्व और उनके यौगिक
आवर्त सारणी के समूह 1 में तत्व शामिल हैं: लिथियम, सोडियम, पोटेशियम, रूबिडियम, सीज़ियम और फ्रांसियम।
समूह 2 के तत्वों में बेरिलियम, मैग्नीशियम, कैल्शियम, स्ट्रोंटियम, बेरियम और रेडियम शामिल हैं।
हाइड्रेशन एन्थैल्पी:
आयनिक आकार में वृद्धि के साथ क्षार धातु आयनों की जलयोजन एन्थैल्पी कम हो जाती है। $\mathrm{Li}^{+}$इसमें जलयोजन की अधिकतम डिग्री होती है और इसी कारण से लिथियम लवण अधिकतर हाइड्रेटेड होते हैं, उदाहरण के लिए, $\mathrm{LiCl} .2 \mathrm{H}_{2} \mathrm{O}$
भौतिक गुण:
सभी क्षार धातुएँ चाँदी जैसी सफेद, मुलायम और हल्की धातुएँ हैं। बड़े आकार के कारण इन तत्वों का घनत्व कम होता है। क्षार धातुओं का गलनांक और क्वथनांक कम होता है जो क्षार धातुओं के कमजोर धात्विक बंधन का संकेत देता है और उनके लवण ऑक्सीकरण ज्वाला को विशिष्ट रंग प्रदान करते हैं।
रासायनिक गुण:
क्षार धातुएँ अपने बड़े आकार और कम आयनीकरण एन्थैल्पी के कारण अत्यधिक प्रतिक्रियाशील होती हैं।
हवा के प्रति प्रतिक्रियाशीलता:
वे ऑक्सीजन में तीव्रता से जलकर ऑक्साइड बनाते हैं। लिथियम मोनोऑक्साइड बनाता है, सोडियम पेरोक्साइड बनाता है, अन्य धातुएं सुपरऑक्साइड बनाती हैं।
प्रकृति को कम करना:
क्षार धातुएँ प्रबल अपचायक हैं, लिथियम सबसे अधिक और सोडियम सबसे कम शक्तिशाली है।
तरल अमोनिया में घोल:
क्षार धातुएँ तरल अमोनिया में घुलकर गहरा नीला घोल देती हैं जो प्रकृति में संवाहक होती हैं।
$ M+(x+y)NH_3 \longrightarrow [M(NH_3)_x]^+ + [e(NH_3)_y]^-$
विलयन का नीला रंग अमोनियायुक्त इलेक्ट्रॉन के कारण होता है और विलयन अनुचुंबकीय होता है।
$ M^+ (am) + e^- + NH_3 (l) \xrightarrow{ \text{on standing }} MNH_2 (am) + 1/2 H_2(g) $
सांद्र विलयन में, नीला रंग कांस्य रंग में बदल जाता है और प्रतिचुंबकीय बन जाता है।
लिथियम के असामान्य गुण
(i) इसके परमाणु और आयन का असाधारण रूप से छोटा आकार, और (ii) उच्च ध्रुवीकरण शक्ति (यानी, चार्ज/त्रिज्या अनुपात)।
लिथियम और मैग्नीशियम के बीच समानता विशेष रूप से हड़ताली है और उनके समान आकार के कारण उत्पन्न होती है: परमाणु त्रिज्या, $\mathrm{Li}=152 \mathrm{pm}, \mathrm{Mg}=160$ अपराह्न; आयनिक त्रिज्या: $\mathrm{Li}^{+}=76 \mathrm{pm}, \mathrm{Mg}^{2+}=72 \mathrm{pm}$.
समूह 2 तत्व: क्षारीय पृथ्वी धातुएँ
पहला तत्व बेरिलियम बाकी सदस्यों से भिन्न है और एल्यूमीनियम से विकर्ण संबंध दर्शाता है।
हाइड्रेशन एन्थैल्पीज़
क्षारीय पृथ्वी धातु आयनों की जलयोजन एन्थैल्पी। $\mathrm{Be}^{2+}>\mathrm{Mg}^{2+}>\mathrm{Ca}^{2+}>$ $\mathrm{Sr}^{2+}>\mathrm{Ba}^{2+}$. क्षारीय पृथ्वी धातु आयनों की जलयोजन एन्थैल्पी क्षार धातु आयनों की तुलना में बड़ी होती है। इस प्रकार, क्षारीय पृथ्वी धातुओं के यौगिक क्षार धातुओं की तुलना में अधिक व्यापक रूप से हाइड्रेटेड होते हैं, उदाहरण के लिए, $ MgCl_2 $ और $ CaCl_2 $ के रूप में मौजूद हैं $ MgCl_2.6 H_2O $ और $ CaCl_2.6H_2O $ जबकि $NaCl$ और $KCl$ ऐसे हाइड्रेट न बनाएं.
भौतिक गुण
क्षारीय पृथ्वी धातुएँ, सामान्यतः, चांदी जैसी सफेद, चमकदार और अपेक्षाकृत नरम होती हैं लेकिन क्षार धातुओं की तुलना में कठोर होती हैं। आकार में छोटी होने के कारण इन धातुओं का गलनांक और क्वथनांक अधिक होता है। कम आयनीकरण एन्थैल्पी के कारण वे प्रकृति में अत्यधिक विद्युत धनात्मक होते हैं। बेरिलियम और मैग्नीशियम में इलेक्ट्रॉन लौ से उत्तेजित होने के लिए बहुत अधिक बाध्य होते हैं। इसलिए ये तत्व लौ को कोई रंग नहीं देते हैं।
कैल्शियम, स्ट्रोंटियम और बेरियम लौ को विशिष्ट रंग प्रदान करते हैं।
रासायनिक गुण
हवा और पानी के प्रति प्रतिक्रियाशीलता:
बेरिलियम और मैग्नीशियम ऑक्सीजन और पानी के प्रति निष्क्रिय हैं। मैग्नीशियम अधिक विद्युत धनात्मक है और हवा में चमकदार चमक के साथ जलता है $\mathrm{MgO}$ और $ Mg_3 N_2 $. ऑक्साइड और नाइट्राइड बनाने के लिए कैल्शियम, स्ट्रोंटियम और बेरियम पर हवा द्वारा आसानी से हमला किया जाता है।
प्रकृति को कम करना:
क्षारीय पृथ्वी धातुएँ प्रबल अपचायक होती हैं। यह उनकी कमी की संभावनाओं के बड़े नकारात्मक मूल्य से संकेत मिलता है।
तरल अमोनिया में घोल:
क्षारीय पृथ्वी धातुएँ तरल अमोनिया में घुलकर गहरा नीला काला घोल बनाती हैं और अमोनियायुक्त आयन बनाती हैं।
$ M+(x+y)NH_3 \longrightarrow [M(NH_3)_x]^{+2} + 2[e(NH_3)_y]^-$
इन समाधानों से, अमोनियाएट्स, $ [ M(NH_3)_6 ]^{+2} $पुनर्प्राप्त किया जा सकता है.
बेरिलियम का असामान्य व्यवहार
समूह 2 धातुओं का पहला सदस्य बेरिलियम, मैग्नीशियम और बाकी सदस्यों की तुलना में असामान्य व्यवहार दिखाता है। इसके अलावा, यह एल्यूमीनियम से विकर्ण संबंध दर्शाता है।
बेरिलियम और एल्युमीनियम के बीच विकर्ण संबंध
की आयनिक त्रिज्या $\mathrm{Be}^{2+}$ होने का अनुमान है $31 \mathrm{pm}$; चार्ज/त्रिज्या अनुपात लगभग समान है $\mathrm{Al}^{3+}$ आयन. इसलिए बेरिलियम कुछ मायनों में एल्यूमीनियम जैसा दिखता है।
एस-ब्लॉक तत्वों के यौगिक
1. सोडियम ऑक्साइड $ ( Na_2O ) $
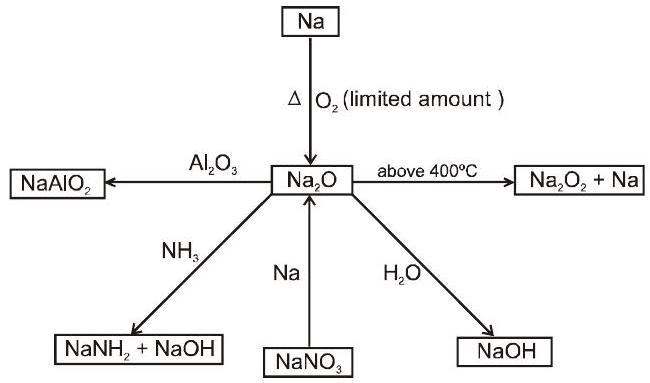
2. सोडियम पेरोक्साइड $ ( Na_2 O_2 ) $
3. सोडियम हाइड्रॉक्साइड (NaOH)
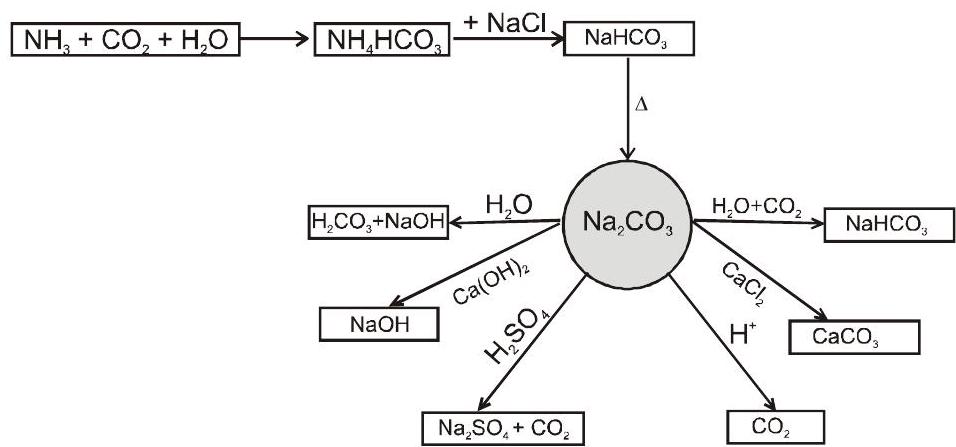
4. सोडियम कार्बोनेट $ ( Na_2 CO_3 ) $
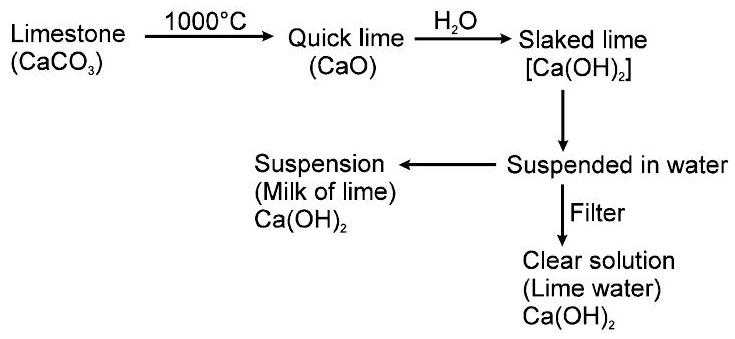
5. बिना बुझा हुआ चूना, बुझा हुआ चूना और नीबू का पानी